文. 许柯
( k7 x9 a! g! ?! Z9 }+ p5 N4 W% L
近日,德国默克宣布终止PD-L1/TGF-β双抗Bintrafusp alfa(M7824)的肺癌三期临床研究(INTR@PIDLung 037)。研究人员在对中期数据进行分析后认为M7824无法击败K药,因此决定提前终止该试验。
) @ I& Y6 Z2 b8 m- b# t) o
“神药”M7824的前世今生
! T" X: d" b& A3 }2018年的美国临床肿瘤学会(ASCO)上默克公司的一款在研新药M7824备受瞩目。
k- g. j- ~. z) C7 F& H4 d8 m根据当时的研究,在非小细胞肺癌患者群体中,M7824取得了良好的治疗效果:给药剂量为500mg,PD-L1+总体缓解率(ORR)为22.6%,PD-L1高表达患者ORR为33.3%。给药剂量为1200mg时,PD-L1+总体缓解率达到了40.7%,而在PD-L1高表达患者中,总体缓解率(ORR)则高达71.4%!
, `3 P r+ Q* `& |5 b1 ~! C7 t
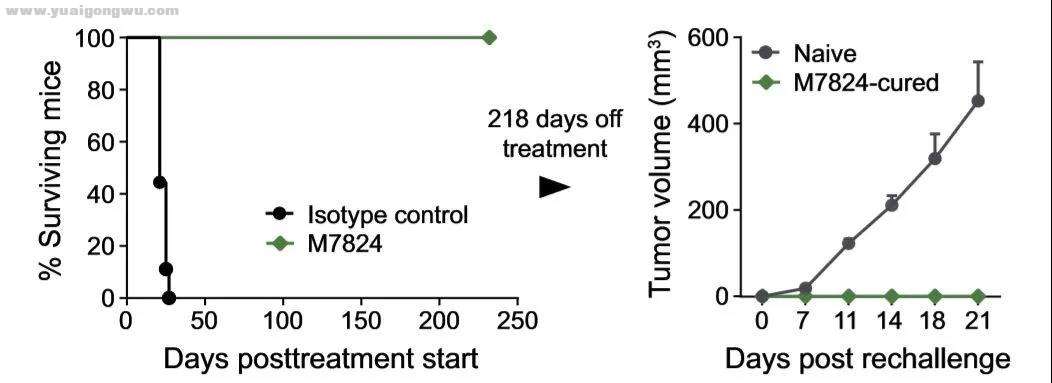
& A( ^8 b! ?$ l/ v, ~5 t( p! G) G并且在动物实验中,M7824的有效率更是达到了惊人的100%。在乳腺癌小鼠模型中长达218天的治疗期,M7824治疗组的小鼠无一死亡,相比较对照组21天的生存中位数,M7824生存曲线数据很好,并且在治疗期间成功的控制住了肿瘤的体积。
$ j$ D- Q8 F- N2 y2 [: l1 m
 7 k' `# W% y& f# [5 T1 o0 {
7 k' `# W% y& f# [5 T1 o0 {
- n0 V& ~ u! D$ g+ Y. U
为什么M7824能一问世便如此惊艳呢?除了良好的治疗效果还要归功于其独特的药物设计。
0 m. s: l( J& z$ J3 C原来M7824相当于是PD-1的升级增强版,它可以同时拮抗TGF-β与PD-L1,相当于同时作用PD-1和TGF-β两个靶点。两个靶点同时起效又具有协同作用,能大幅提高治疗的有效率。此外,TGF-β或许可以克服肿瘤细胞对PD-1/PD-L1疗法的抗药性。
$ h T+ U& V6 p: ?, m
) X% |! d" j% j6 p' D# i- Z; {因此,M7824也被称为二代PD-1。
0 v1 U2 N; R2 _$ \/ W2 u
此时的M7824可谓是风光无两,不仅成为了医药界集体关注的新宠,也成了患者翘首以盼的福音。
! F+ W& t" S6 [3 M, Q) B9 U c
顺理成章的M7824也就开始了全方位地发展,在结直肠癌、胃癌、HPV阳性肿瘤、肺癌等多种领域都展开了相应的研究。
( l( L2 V+ L3 z
突然间的土崩瓦解
7 W, i; T8 X4 }2 K. o去年4月,从JTO杂志上公布的临床研究结果来看,M7824的研究结果似乎还是符合预期的。
: t0 x7 x, L# b4 v
7 h9 V1 F: P0 }' `9 o此次在JTO上更新的试验数据是基于NCT02517398Ⅰ期临床试验,该研究旨在探索M7824在晚期NSCLC二线治疗临床疗效。
. R% Y4 w% x l, u试验共纳入了80例既往铂类化疗进展的晚期非小细胞肺癌患者。受试者按1:1随机接受500mg或1200mg(Ⅱ期临床推荐剂量)的M7824治疗。PDL1表达检测为,72.5%为PDL1阳性,16.3%为PDL1高表达(≥80%)。78.8%的患者既往接受过一线治疗,其余接受过二线及以上治疗方案。
6 d/ |" W0 b; d
在总人群中,客观缓解率(ORR)为21.3%,疾病控制率(DCR)为40%,中位缓解持续时间(DOR)为14.1个月。
& m8 S4 G" `* |总人群的中位无进展生存期(PFS)为1.6个月,500mg及1200mg组的PFS分别为1.4个月和2.7个月。
; Q9 ^2 U; g2 a, j9 p
) ]3 d. V3 l) R总人群的中位总生存期(OS)为13.6个月,500mg/1200mg组的OS分别为10.9个月和15.6个月。
+ D+ S+ W e: g! e$ T
0 m9 S6 i8 K1 c) I, {. [
值得一提的是在1200 mg剂量下,PD-L1阳性患者客观缓解率达到37.0%,而对于PD-L1高表达的患者的客观缓解率高达85.7%。
4 V5 _ u+ l+ P
9 J. z, f2 d$ f" n从2020年CSCO大会上更新的数据来看,M7824的有效率与生存时间都要显著优于一代的PD-1。
) U3 J- C% b$ Y' t# zITT总人群ORR为23.8%,中位DOR为15.3个月,84.2%患者缓解持续时间超过半年,67.7%的患者缓解持续时间超过1年,呈现有效患者长期起效的优势。1200mg组ORR为27.5%,比初期数据更为显著;中位DOR为18.0个月,72.7%的患者疗效持续超过半年,63.6%的患者疗效持续超过1年。
J* L6 |* B' J) V4 l/ s' C. l0 Q, X& k1 [- J
1200mg组,ITT人群的中位OS 为17.1个月,PD-L1阴性(<1%)患者中位OS为12.2个月,PD-L1阳性患者中位OS为21.7个月。
/ H8 `: L5 ?0 P: Q4 [
' _, I& |3 Z6 c1 C1 |8 N" v
, e0 n/ s6 _$ Z. J& I
在2020年ESMO大会上公布的研究数据显示,40位患者接受了1200 mgM7824治疗的非小细胞肺癌患者,经过3年的随访,12、24和36个月的OS率分别为66.2%,39.7%和23.2%。PD-L1阳性患者的36个月OS率为33.6%,PD-L1高表达患者为66.7%。
% X+ Q: Y. p5 q然而,这栋我们亲眼看着一点点矗立起来的大楼又在我们的注视下坍塌了。曾经各种优异的数据就如同美丽的泡沫般一触就破。留给我们的只剩无尽的惋惜。; u' ^5 }9 y: i
+ c O F% h, T' }1 t; Q
二代PD-1路在何方?
' X+ m3 ~' Q6 a1 ?从惊艳的问世,到后续不断更迭的亮眼表现,再到如今肺癌研究的提前落幕,M7824是不是真的被我们高估了呢?为什么前期的顺风顺水试验突然就宣告终止?那些还在进行的M7824其他适应症的研究前途又是否光明呢?
' T4 v4 D- {" y关于M7824的种种疑问我们很难去找到答案。美梦破灭的背后是我们对二代PD-1操之过急了吗?
; q# o# V0 t! v9 P! ?2 U- A* |) F3 y7 `
+ Q2 `2 P9 k8 T
但眼看着靶向药一代代的更迭,更好的疗效,处理前代的耐药,这些我们真的也想在免疫治疗上看到。
9 F" ]9 b2 o$ ], E- }; i
希望默克公司能从失败中吸取教训,尽快发现失败的原因,在其他适应症上能给出好的结果。
8 l$ f6 N3 o! r总之,此次M7824肺癌试验的终止既是给我们泼了盆冷水也是给我们上了一课:并不是所有的“神药”最后都能取得好的结果,只有审批上市才是评判它安全可靠的真正标准,不然期望有多大最后失望就有多大。
$ @4 `# v8 Q+ F2 ]- `
9 E3 P; d7 G- Q& M S
" v8 Z8 l3 `& k& y4 D1 K/ J! J